Coronavírus
Governo vai enviar doses pediátricas para Estados com baixos estoques
Paraná está entre as regiões
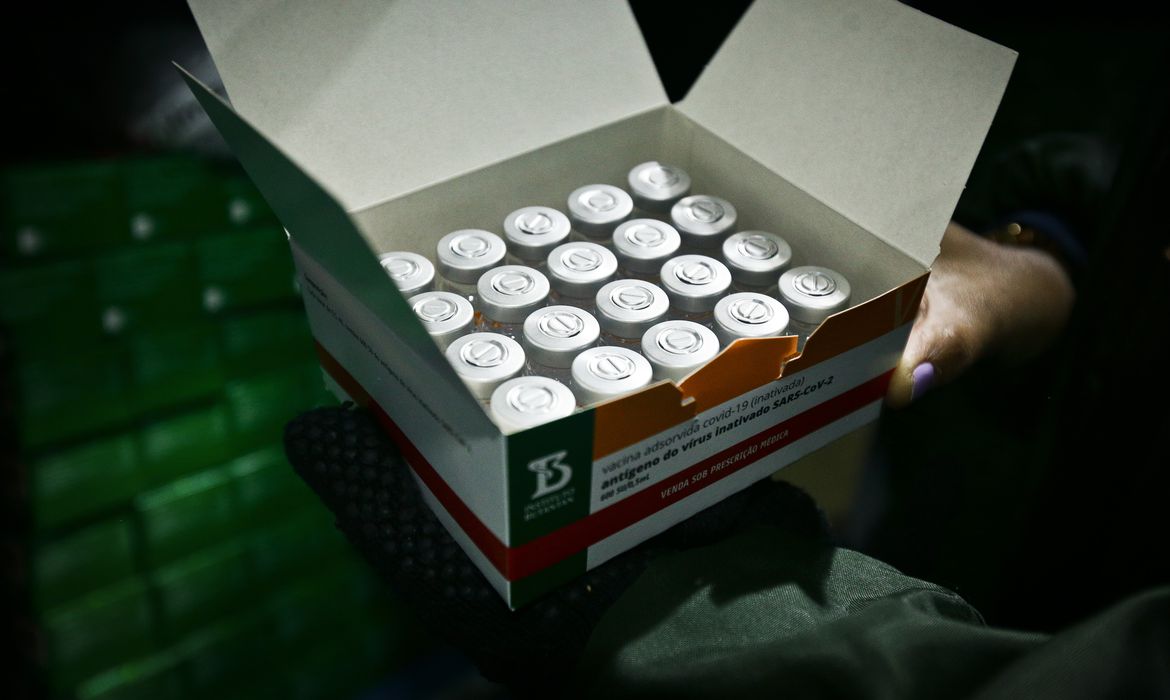
O Ministério da Saúde anunciou o envio de uma remessa emergencial de vacinas para crianças a Estados com estoques abaixo das 40 mil doses para a aplicação no público infantil.
Segundo a pasta, doze Estados estão nessa situação: Mato Grosso do Sul, Mato Grosso, Pernambuco, Sergipe, Amapá, Acre, Pará, Roraima, Tocantins, Rio de Janeiro, Paraná e Santa Catarina.
O secretário executivo do órgão, Rodrigo Cruz, informou que a remessa emergencial abrangerá uma quantidade de doses suficiente para imunizar 10% do público-alvo infantil de cada Unidade da Federação nessa situação.
CoronaVac
Em entrevista coletiva na sede da pasta, o secretário executivo confirmou a inclusão da vacina CoronaVac para crianças e adolescentes de 6 a 17 anos no Plano Nacional de Operacionalização de Vacinação Contra a Covid-19.
O Ministério abriu negociações com o Instituto Butantan, responsável pela produção do imunizante em parceria com a farmacêutica chinesa Sinovac. A pasta foi informada pelo instituto de que há sete milhões de doses disponíveis.
Cruz explicou que o órgão irá consultar os Estados para saber se há necessidade de compra de novas doses. O ministério possui seis milhões de doses em estoque e, os Estados, outros três milhões. Caso haja necessidade, a negociação poderá prosseguir.
Esse cálculo envolve também as doses da vacina pediátrica da Pfizer. O Ministério da Saúde já contratou 20 milhões de doses e começou a negociar outros 10 milhões. Mas a CoronaVac pode ter preferência por ter possibilidade de entrega em pouco tempo.
“A gente discute a pertinência de receber esses 10 milhões dado que houve aprovação da CoronaVac e tem disponibilização mais imediata. Podemos jogar 10 milhões da Pfizer para o futuro”, explicou Cruz.
As doses da vacina pediátrica da Pfizer seguirão sendo distribuídas aos Estados. Uma nova remessa de 1,2 milhão de doses já foi enviada e outra remessa, com a mesma quantidade, está prevista para o dia 3 de fevereiro.
Autotestes
Na entrevista coletiva, Rodrigo Cruz comentou também a reunião entre o Ministério da Saúde e Agência Nacional de Vigilância Sanitária (Anvisa) sobre autotestes. A diretoria da agência negou a liberação da comercialização de testes por leigos pela falta de informações do Ministério sobre qual será a política pública para o tema.
A diretoria da Anvisa aprovou o envio de questionamentos à pasta e um prazo de 15 dias para uma nova apreciação do tema. Rodrigo Cruz disse que a reunião tratou de temas para viabilizar as normas para os autotestes, como quem poderia comprar, a forma de uso, o fluxo dos pacientes, os canais de atendimento e as campanhas de esclarecimento.
“Tratamos de alguns assuntos para poder aprimorar a documentação do Ministério e avançar no objetivo comum, que imagino que seja a aprovação dos autotestes como apoio à testagem. Acho que estamos bem alinhados com relação ao autoteste e estamos com meta para mandar contribuições para que possamos formalizar novo pleito para a diretoria colegiada possa analisar”, disse o secretário executivo.
Com informações da Agência Brasil




























