Coronavírus
Anvisa recebe informações de todas as vacinas em uso no Brasil sobre eficácia contra a Ômicron
Avaliação da efetividade contra a variante deverá levar semanas ou meses
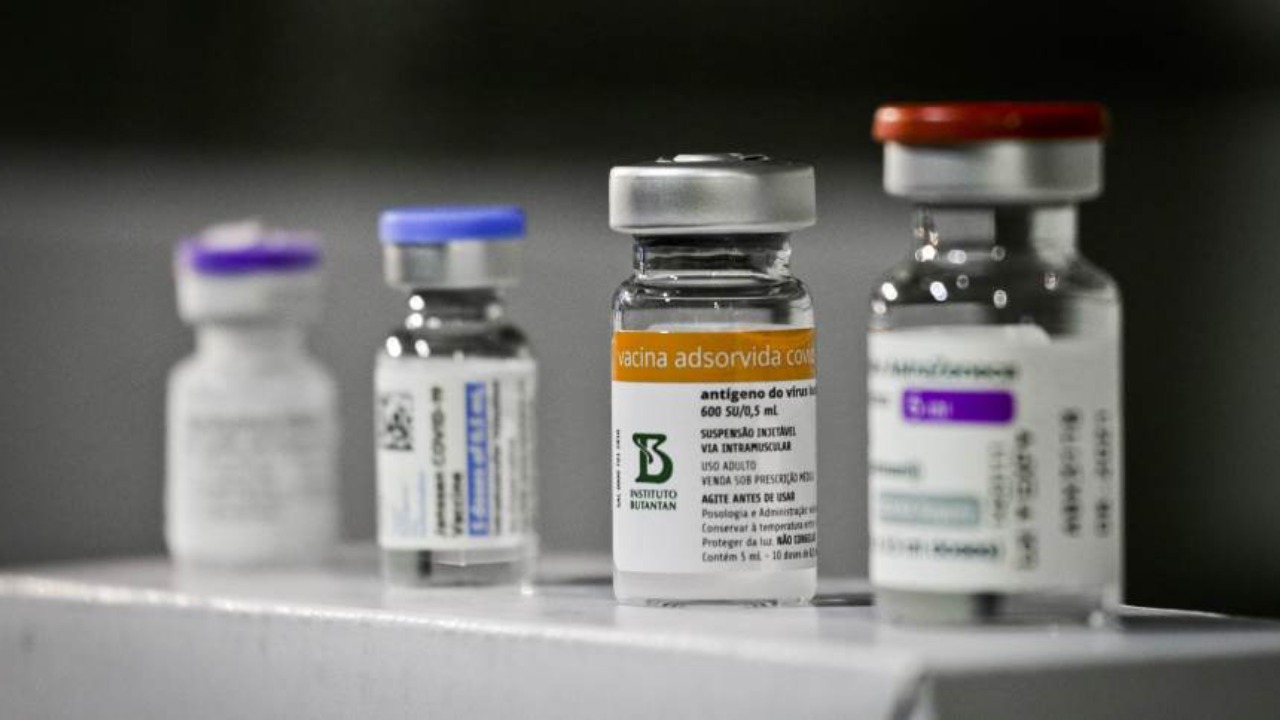
Na última quarta-feira, 8, a Agência Nacional de Vigilância Sanitária (Anvisa) divulgou atualização sobre a avaliação das vacinas contra a Covid-19 que estão sendo utilizadas para imunização no Brasil frente à nova variante da Ômicron. A agência solicitou a todas as desenvolvedoras da AstraZeneca, CoronaVac, Janssen e Pfizer, informações sobre a eficácia contra a variante, algo que foi repassado na última semana e será analisado nas próximas semanas e meses para uma conclusão científica. A Anvisa ainda reforçou que os imunizantes prosseguem sendo a melhor forma de defesa contra o vírus.
“A Anvisa solicitou às desenvolvedoras de vacinas autorizadas no Brasil, no último dia 1º de dezembro, informações sobre os estudos em andamento. A solicitação foi encaminhada aos laboratórios Pfizer, Butantan, Fiocruz e Janssen. A agência exige, para as vacinas autorizadas, que os desenvolvedores monitorem e avaliem o impacto das variantes na eficácia e na efetividade dos imunizantes. É preciso observar, porém, que esses estudos demandam tempo, uma vez que é preciso obter informações genéticas e amostras de pacientes para então realizar os testes e a análise”, informa a assessoria da Anvisa.
Segundo a agência, foi dado o prazo de uma semana para todas as empresas se manifestarem, sendo que a situação atual é a seguinte: “a Pfizer, a Fiocruz, o Instituto Butantan e a Janssen encaminharam as estratégias que estão sendo tomadas, em resposta ao ofício”, completa. “A Gerência-Geral de Medicamentos e Produtos Biológicos (GGMED) avaliará os dados encaminhados e continuará o monitoramento dos estudos relativos à variante Ômicron”, informa.
De acordo com a Anvisa, o cenário epidemiológico da prevalência da Ômicron está sendo acompanhado, sendo que “a ausência das informações solicitadas pode prejudicar a manutenção da atual autorização da Anvisa”, complementa. “É importante esclarecer que a avaliação experimental completa da Ômicron pode levar semanas ou até meses. Entretanto, os desenvolvedores de vacinas devem manter a vigilância permanente dos seus imunobiológicos frente ao aparecimento dessa variante que causa preocupação”, explica.
Vacina segue sendo principal linha de defesa
Segundo a agência nacional, a nova variante conta com muitas alterações na proteína spike, assim como mutações em outras partes do genoma viral, sendo que as indicações iniciais sugerem que a Ômicron pode ser mais transmissível. “A Anvisa reforça, baseada em tudo o que se sabe até o momento, que as vacinas continuam sendo a nossa melhor linha de defesa e que todos aqueles que ainda não receberam a primeira ou segunda dose da vacina, ou que são elegíveis para a dose de reforço, são encorajados a se apresentarem para ajudarem a proteger a si próprios e ao coletivo”, acrescenta.
“O programa de vacinação, a ampla testagem, o rastreamento genômico e a adoção das medidas não farmacológicas (uso de máscaras, distanciamento social, higienização das mãos) continuam sendo essenciais para o enfrentamento da pandemia, independentemente da variante Ômicron. A Anvisa manterá o trabalho ativo com os reguladores internacionais e desenvolvedores dos imunizantes para possibilitar uma atuação rápida diante de potenciais impactos da nova variante Ômicron nas vacinas contra Covid-19 usadas no Brasil”, finaliza a Anvisa.
Com informações da Anvisa




























